济南实验室王杭祥团队在《Journal of Clinical Investigation》期刊发表STING激动剂诱导的肿瘤免疫逃逸及治疗新策略研究成果
济南实验室王杭祥教授团队在肿瘤免疫治疗领域取得重要突破,该研究不仅精准揭示了STING激动剂临床应用受限的关键机制,更通过结构导向的理性药物设计与精准纳米组装技术,成功构建出"免疫调节二元纳米粒"(Immunomodulatory binary nanoparticles, iBINP)——该创新制剂能够主动靶向并重塑肿瘤免疫微环境,有效逆转STING通路过度激活介导的免疫耐受,该制剂首次实现了STING激动剂的静脉递送,突破了该类药物必须瘤内注射的临床限制,同时为解决STING疗法引发的适应性免疫逃逸提供了全新的技术路径。该成果以“Targeting STING–induced immune evasion with nanoparticulate binary pharmacology improves tumor control in mice”为题,于2025年10月23日在《Journal of Clinical Investigation》杂志在线发表研究论文。
干扰素基因刺激蛋白(STING)激动剂疗法是肿瘤免疫领域最具潜力的策略之一。STING通路能够激活机体天然免疫系统,将免疫“冷肿瘤”转化为“热肿瘤”,从而使免疫细胞得以浸润并杀伤癌细胞。尽管STING激动剂在临床前研究中显示出卓越的抗肿瘤活性,其临床疗效却不尽人意。STING激动类药物的临床应用的耐药及免疫逃逸机制是亟待解决的问题。
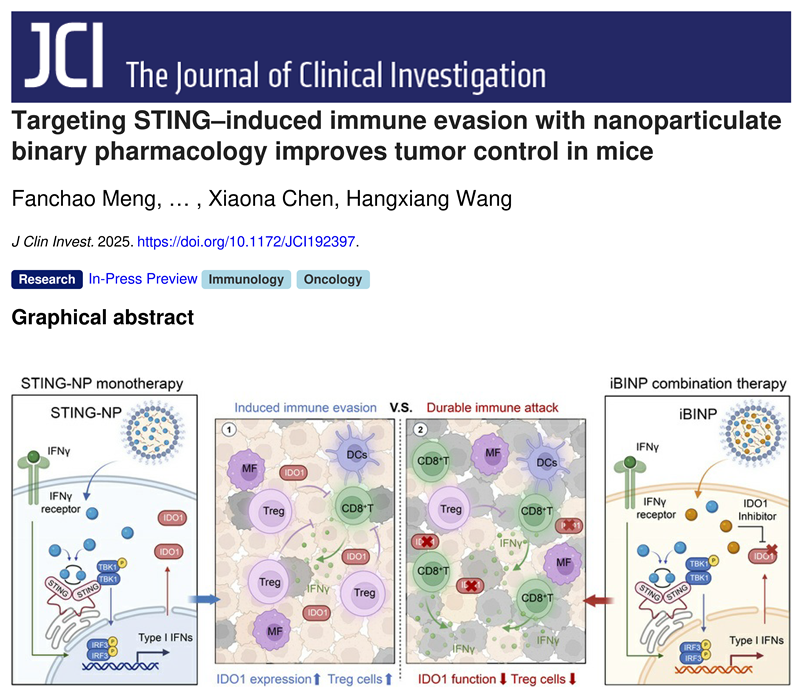
本研究首先提出了一个关键的科学问题:为什么STING激动剂的疗效会自我设限?通过多种组学分析和一系列的机制验证,团队发现STING激动剂在激活I型干扰素通路的同时,会诱导促进免疫耐受和逃逸的负反馈环路。具体而言,STING激动剂诱导产生的IFN-γ导致肿瘤微环境中关键免疫代谢检查点——吲哚胺2,3-双加氧酶1(IDO1)——的高表达和功能上调。IDO1代谢酶通过调控色氨酸/犬尿氨酸代谢途径,创造了一个免疫抑制的肿瘤微环境,促进调节T细胞的分化,从而抑制效应T细胞的功能并诱导其凋亡,最终导致STING激动剂治疗时的免疫逃逸。为了证实IDO1是介导STING激动剂耐药的关键开关,研究团队构建了 Ido1 敲除和 Ido1 过表达的肿瘤模型。实验结果表明:在Ido1过表达的肿瘤模型中,STING药物的疗效被显著削弱;而在Ido1敲除的肿瘤模型中,单STING激动剂的药物活性则与iBINP相当(图1)。这一关键实验证明了IDO1表达水平的上调是介导STING激动剂耐药的核心机制。
针对该负反馈机制,研究团队设计并构建了一种“二元前药共组装”策略,将两种理化性质迥异、难溶性及无法用于静脉递送的小分子化合物——STING激动剂(MSA-2)和IDO1抑制剂(NLG919)——分别进行脂质化修饰。这种分子水平的结构重构使得两种不同的前药能够通过超分子非共价相互作用,共组装形成可静脉滴注给药、并在血液中长循环的新型免疫调控纳米药物(iBINP)。该递送系统的独创性在于并非简单的药物联用,而是通过巧妙的药物化学和创新制剂策略,高效解决了多种不同药物之间相互协同的关键难题。更为关键的是,iBINP确保不同药物分子能够在肿瘤部位和引流淋巴结实现时空共递送,也是其发挥协同作用的先决条件(图1)。
该iBINP药物系统在多种难治性肿瘤模型中均展现了较好的活性。在结直肠癌和乳腺癌皮下瘤模型中,iBINP的治疗窗和疗效显著优于两种药物的单药或游离药物联用。更有意思的是,在本团队构建的STING药物获得性耐药肿瘤模型中,STING激动剂单一疗法已丧失肿瘤抑制效果,但iBINP却能高效抑瘤,并显著延长生存期,成功缓解了STING药物诱导的肿瘤免疫逃逸与耐受(图1)。此外,该策略在难治性的结肠炎相关性癌症(CAC)模型和术后肺转移模型中也表现出卓越的治疗潜力。
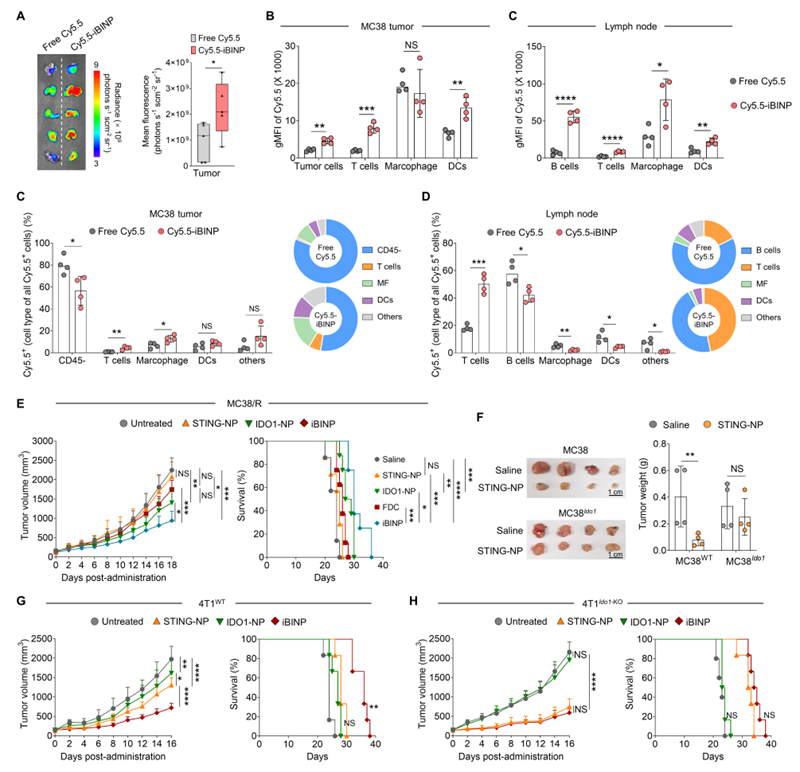
图1、iBINP的体内生物分布及抗肿瘤机制验证。(A)静脉注射Cy5.5标记的iBINP或游离Cy5.5染料后的离体肿瘤组织的荧光成像图。(B, C)流式细胞术分析iBINP在MC38肿瘤(左)和肿瘤引流淋巴结(右)中各类细胞的摄取情况比较图。(D)MC38肿瘤(左)和肿瘤引流淋巴结(右)中Cy5.5染料标记的iBINP药物细胞类型分布图及占比分析。(E)STING激动剂获得性耐药(MC38/R)皮下瘤模型中各治疗组小鼠的肿瘤生长曲线和生存分析。(F)STING激动剂(STING-NP)治疗MC38野生型(MC38WT)和Ido1过表达的MC肿瘤(MC38 Ido1)后的离体肿瘤比较图和统计图。(G, H)野生型4T1(4T1WT)和Ido1基因敲除(4T1Ido1-KO)的4T1皮下瘤模型中各治疗组的肿瘤生长曲线和小鼠生存期。
综上所述,本研究不仅揭示了STING药物抗肿瘤的耐药机制,而且提供了基于合成化学和超分子化学的新型纳米药物(iBINP)策略来解决这一负反馈环路。iBINP在体内发生降解,仅生成两种药物及对人体非常重要的多不饱和脂肪酸——DHA。该研究为STING激动剂的临床转化提供了新的解决方案,临床转化价值高。
科研启发:本工作创新性地提出了"机制导向的协同递送"设计理念,通过解析药物作用过程中的负反馈环路,针对性构建具有时空协同效应的纳米药物,为克服肿瘤免疫治疗的耐药性问题提供了新范式。
王杭祥教授课题组长期从事抗肿瘤免疫药物和递送系统的基础和临床转化研究。近年已在PNAS、Cancer Res.、Nat. Commun.、Adv. Mater.、ACS Nano、Biomaterials、J. Controlled Release等学术期刊发表论文100多篇,部分创新药成果已转让并进入临床转化阶段。本研究获得了济南微生态生物医学省实验室项目(编号:JNL-2025007B)、山东省自然科学基金重大基础研究项目及国家自然科学基金委面上项目等经费的资助。