济南实验室王杭祥教授团队在线粒体靶向光动力免疫治疗领域取得新进展
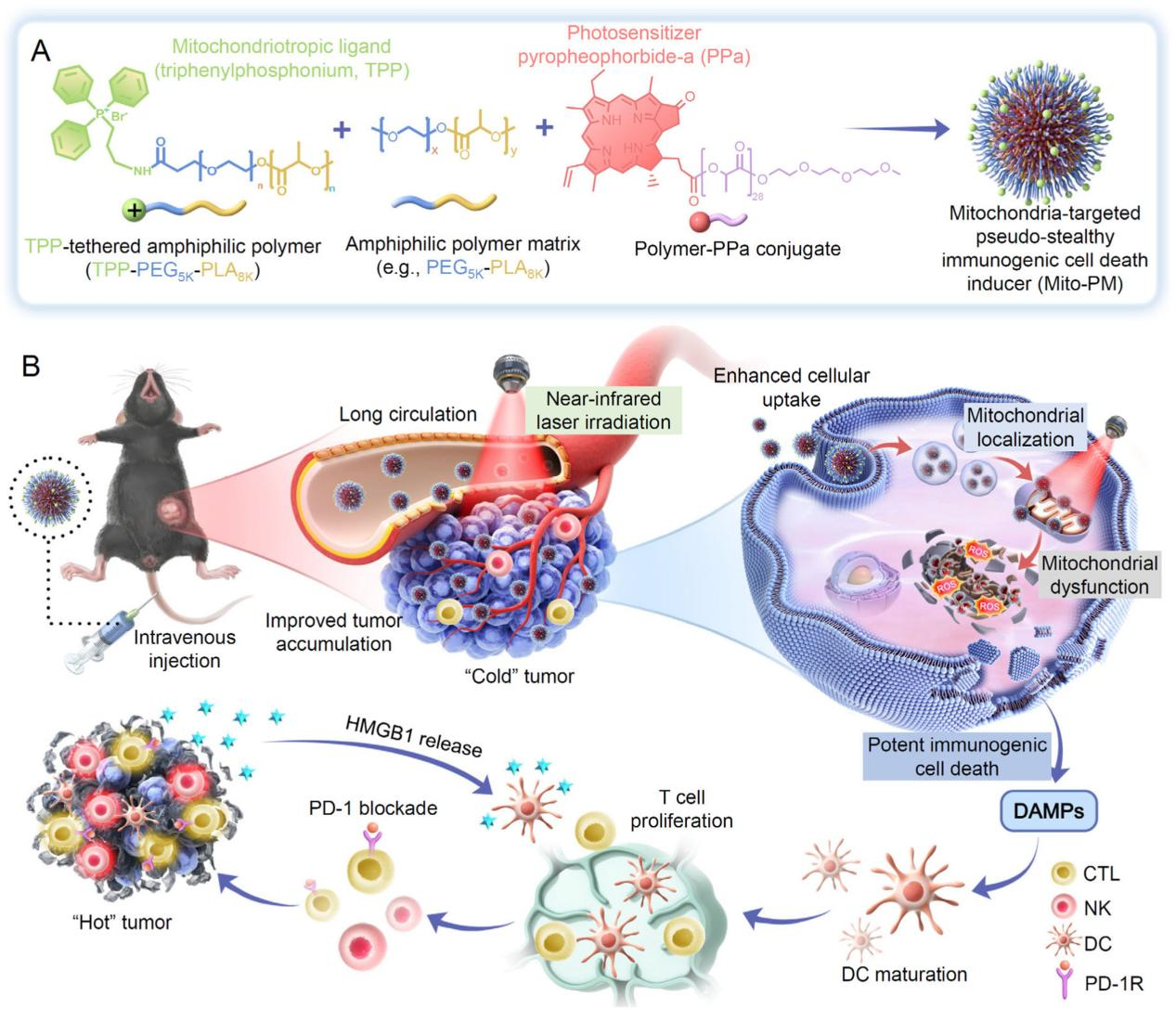
近日,济南微生态生物医学省实验室王杭祥教授团队针对黑色素瘤对免疫检查点抑制剂响应率低的难题,基于线粒体靶向诱导免疫原性细胞死亡(ICD)的机制,开发了一种线粒体靶向的“伪隐形”纳米光敏剂新策略,通过高效破坏肿瘤细胞线粒体并激活系统性抗肿瘤免疫,显著增强免疫治疗效果。该研究以“Mitochondria-targeting pseudo-stealthy nanophotosensitizer as a potent immunogenic cell death inducer to unleash the cancer-immunity cycle for melanoma therapy”为题在《Acta Biomaterialia》杂志发表。

黑色素瘤起源于黑色素细胞,是最具侵袭性的癌症之一。免疫检查点抑制剂(如抗PD-1/PD-L1)虽已成为黑色素瘤治疗的重要手段,但约50%患者因肿瘤微环境中T细胞浸润不足、免疫抑制因子富集等问题,难以从中获益。线粒体作为细胞的“能量工厂”,同时也是调控免疫应答的关键枢纽。靶向线粒体可诱导肿瘤细胞释放大量损伤相关分子模式(DAMPs),触发强烈的免疫原性细胞死亡(ICD),激活树突状细胞(DC)成熟及T细胞抗肿瘤反应。传统光动力疗法(PDT)虽能诱导ICD,但存在光敏剂靶向性差、易被快速清除、肿瘤穿透不足等问题。
研究团队创新性地设计了Mito-PM胶束纳米平台,通过在纳米胶束表面低密度地修饰三苯基膦(TPP)阳离子,确保了胶束在血液循环中的长滞留和肿瘤高蓄积,同时又使其能借助于TPP通过线粒体膜电位差高效富集于肿瘤细胞的线粒体。在近红外光(660 nm)照射下产生大量活性氧(ROS),直接破坏线粒体结构,诱导强效的ICD。通过细胞实验证实,Mito-PM可以特异地靶向细胞线粒体,引起线粒体的功能障碍,诱导细胞ICD。在B16F10动物模型上,Mito-PM联合anti-PD-1抗体展现出显著的协同治疗效果。结果显示Mito-PM组肿瘤体积显著小于非线粒体靶向光照组,而联合anti-PD-1抗体治疗实现最佳抑瘤效果,第15天肿瘤体积较anti-PD-1单药组显著缩小。病理分析显示,联合治疗组表现出明显的肿瘤细胞凋亡、增殖抑制和免疫细胞浸润,同时ICD也被显著激活。
上述研究结果证明,在不损害线粒体蓄积的前提下降低纳米胶束的表面正电荷修饰密度,可有效改善胶束的药代动力学特性;线粒体靶向的光动力疗法不仅能增强抗肿瘤免疫应答、提高治疗效果,还能与免疫检查点抑制剂协同作用,从而产生更佳的抗肿瘤疗效。
科研启发:该研究创新性地提出了低密度阳离子修饰的“伪隐形”纳米设计理念,为解决光敏剂靶向性差与免疫激活弱的双重难题提供了新思路,为联合免疫疗法治疗黑色素瘤开辟了新途径。
该研究工作得到了山东省自然科学基金重大基础研究项目(ZR2023ZD59)及济南微生态生物医学省实验室科研项目(JNL-2025007B)等经费的资助。
原文链接:https://www.sciencedirect.com/science/article/pii/S174270612500532X