实验室顾晓松院士、江春平教授、曹毅教授、杨佳鹏助理研究员团队发现细胞在动态软基质上的新型高速迁移模式
近日,继在Cell Stem Cell期刊上发文通过光调控水凝胶揭示细胞可通过力信号分子的积累来感知快速刚度变化后,济南微生态生物医学省实验室顾晓松院士、江春平教授、曹毅教授、杨佳鹏助理研究员联合四川大学魏强教授研究团队,针对软基质环境中的细胞迁移机制问题,进一步首次揭示动态软基质刚度变化通过触发细胞内外力学失衡介导新型高速迁移模式。该研究以“Dynamic Rigidity Changes Enable Rapid Cell Migration on Soft Substrates”为题在Nature Communications(IF:15.7)上发表。

在生物体内,细胞迁移是组织发育、伤口愈合乃至癌症转移等关键生命过程的核心。传统观点认为,细胞更倾向于在较硬的基质上迁移,因为柔软的表面(低于4千帕)无法提供足够的牵引力。然而,许多人体器官组织如肺、肝脏等是柔软且动态变化的,细胞如何在动态环境中高效迁移一直是个未解之谜。
动态刚度变化解锁细胞在软基底上的“迁移密码”
研究团队利用其开发的光响应水凝胶构建了可精确调控的动态力学环境。研究发现,当基底刚度在1.6千帕和2.2千帕之间以1分钟间隔快速循环时,细胞迁移速度提升超过36倍,甚至超过了在13.0千帕静态刚性基底上的传统迁移速度,这颠覆了“细胞在软基底上难以迁移”的传统认知。与传统的、具有明确方向的间充质迁移不同,细胞在动态软基底上展现出独特的“伸长-回弹”(elongation-and-snapback)行为:细胞两端沿随机方向伸长后一端迅速回弹,并不断重复该循环。这种迁移模式无需细胞建立极性,表现出高效但无固定方向的“探索式”运动。
力失衡机制驱动细胞迁移
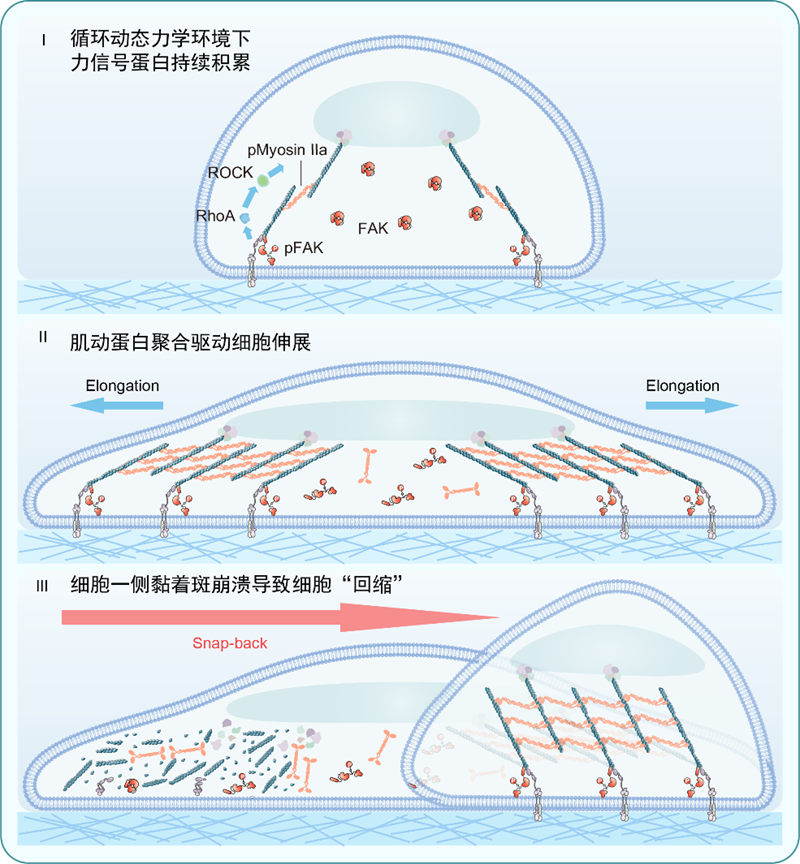
前期研究发现动态刚度循环可导致力信号蛋白积累,从而增强细胞内部收缩力,驱动细胞伸展。这项研究进一步揭示,这种内部收缩力的快速增长打破了细胞内外力平衡。当内部收缩力持续超过外部黏附力时,细胞一侧黏着斑全部崩解,使细胞体迅速“回弹”完成位移。这种由动态刚度诱导的“力失衡”是驱动迁移的核心机制。实验验证中,当通过增强黏附或抑制收缩来“修复”力失衡后,细胞的快速迁移现象随之消失,有力证实了该机制的正确性。
科研启发:
该研究不仅发现了一种全新的细胞迁移模式,还深化了对细胞力学感知机制的理解,表明细胞能巧妙利用环境的动态变化来克服静态限制。在生理层面,这种“探索-稳定”(search-and-settle)的迁移模式有助于细胞在体内快速探索微环境,如在组织修复时迅速离开损伤区域并“定居”于稳定环境。然而,在病理状态下,该机制也可能被癌细胞等“利用”,在力学稳态被破坏的组织中(如癌症或纤维化),使其获得超强的迁移能力,从而增加侵袭和转移的风险。
该研究得到了山东省重点研发计划(SYS202202)、济南微生态生物医学省实验室科研项目(JNL-2023004Q, JNL-2025008B, JNL-2025009B, JNL-2025010B)和山东省自然科学基金(ZR2024QC217)的资助,济南实验室为第一完成单位。